国内首款PI3K抑制剂申报上市获受理,恒瑞、信达都在布局
3月10日,CDE官网显示,拜耳PI3K抑制剂「Copanlisib 注射用冻干制剂」的进口申请获受理。
Copanlisib是一种新颖的静脉注射型泛I类磷脂酰肌醇-3-激酶(PI3K)抑制剂,对恶性B细胞中表达的PI3K-α和PI3K-δ异构体具有主要的抑制活性。2017年9月,该药被FDA加速批准单药用于治疗既往已接受过至少2种系统性疗法的复发性或难治性滤泡性淋巴瘤(FL)成人患者,商品名为Aliqopa 。2019年6月,FDA授予该药突破性药物资格(BTD),用于治疗既往已接受过至少2种疗法的复发性边缘区淋巴瘤(MZL)成人患者。
滤泡性淋巴瘤(FL)和边缘区淋巴瘤(MZL)均属于非霍奇金淋巴瘤(NHL),其中FL是最常见的惰性淋巴瘤,约占所有NHL病例的20%。而FL是第三常见的B细胞NHL,约占所有NHL病例的8%。
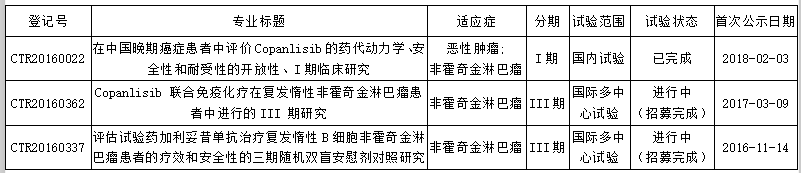
据insight数据库,Copanlisib在国内共登记3项临床试验,详见下表。根据试验进度,笔者尚不能确定该药在国内具体申报哪种适应症,但根据该药在国外的监管状态,估计是边缘区淋巴瘤的可能性比较大。
关于PI3K抑制剂
PI3K,即磷脂酰肌醇3-激酶,是一种胞内脂质磷酸激酶,由p85调节亚基、p55调节亚基和p110催化亚基组成。根据结构和底物的不同,PI3K可分为I型、Ⅱ型和Ⅲ型,其中I型PI3K是由PI3K催化亚基和调控亚基组成的异二聚体,是目前研究最深入、最广泛的亚型,与肿瘤的关系也最为密切。根据催化亚基的不同,I型PI3K又可细分为IA和IB两型,其中IA型PI3K的催化亚基包括p110α、p110β、p110δ三个蛋白,IB型PI3K的催化亚基只有p110γ。不同催化亚基的PI3K表达不同,其中PI3Kα、PI3Kβ在多种细胞中表达,PI3Kδ、PI3Kγ只在免疫系统中表达。
II型和III型PI3K主要控制膜运输,间接调节信号转导。其中II型PI3K成员包括PI3KC2α、PI3KC2β和PI3KC2γ三个亚型,III型PI3K由催化亚基Vps34和调节亚基 Vps15组成。
研究发现,PI3K是人类癌症中最常被激活的信号通路之一,几乎介导50%恶性肿瘤的发生。其信号通路的过度活跃与肿瘤的进展、肿瘤微血管密度的增加、癌细胞的趋化性和侵袭性增强有显著的相关性。由于其在癌症发生和进展中起的重要作用,PI3K已成为研究人员开发癌症靶向药的热门靶点之一。
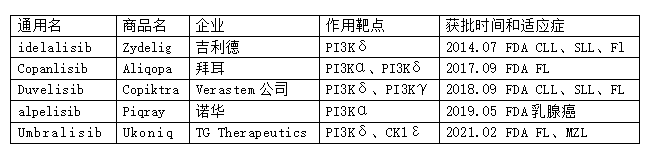
目前,研究人员开发的PI3K抑制剂种类很多,根据作用机制,大致可分为广谱型PI3K抑制剂(pan-PI3K)、亚型特异性PI3K抑制剂和靶向PI3K/mTOR双重抑制剂三大类。据insight数据库,全球总共批准5款PI3K抑制剂,即吉利德的idelalisib、拜耳的copanlisib(Zydelig)、拜耳的Copanlisib(Aliqopa)、Verastem公司的duvelisib(Copiktra)、诺华的alpelisib(BYL719,Piqray)和TG Therapeutics的Umbralisib。
上述5款PI3K抑制剂的作用靶点和适应症存在差异,尤其是诺华的Piqray,它是一款小分子PI3Kα抑制剂,于2019年5月被FDA批准联合氟维司群用于携带PIK3CA基因突变的HR+/HER2-晚期或转移性乳腺癌患者。据悉,大约40%的HR+/HER2-晚期乳腺癌患者携带PIK3CA基因突变。研究发现,与氟维司群单药相比,Piqray联合氟维司群可使患者中位无进展生存期增加近一倍(11.0 vs 5.7 个月)。上市后,Piqray就显示出巨大的市场潜力,上市后不足7个月销售额就达到1.16亿美元,2020年的销售额达3.2亿美元。
Zydelig是全球批准的首款PI3K抑制剂,2014年7月被FDA批准用于治疗3种B细胞血液肿瘤,即联合罗氏利妥昔单抗(Rituxan)用于治疗适合Rituxan单药疗法的复发性慢性淋巴细胞白血病(CLL),以及单药治疗既往接受过至少2种系统治疗方案的复发性滤泡B细胞非霍奇金淋巴瘤(FL)和小细胞淋巴瘤(SLL)。但安全性问题是其不可逾越的障碍,上市时就携带4项黑框警告,提示存在包括致命性肝脏问题在内的风险。2016年因在临床研究中出现感染相关死亡等严重不良事件,先后遭到EMA和FDA的警告和调查。随后吉利德宣布暂停该药的所有临床研究。近年来,Zydelig销售额逐年下滑,2020年仅有0.72亿美元。
Copiktra是FDA批准的首个PI3K-δ和PI3K-γ双效抑制剂,2018年9月被FDA批准用于治疗既往已接受至少2种疗法的复发或难治性(R/R CLL/SLL)成人患者,以及被FDA加速批准用于既往已接受至少2种疗法的复发或难治性FL成人患者。该药几次易主,最初由Intellikine(后被武田收购)研发,后Infinity获得其全球开发和商业化权利。2014年Infinity与艾伯维达成合作协议联合开发Duveraisib,但2016年艾伯维终止与Infinity的合作,Infinity又重新获得该药的全球权利。2016年11月,Infinity又将该药的全球权利独家授权给Verastem(现为Verastem Oncology)。值得一提的是,2018年9月,石药集团与Verastem公司签订协议,获得Copiktra在中国的独家权益,目前在国内处于II期临床试验阶段,适应症为FL。2019年7月,赛诺菲与Verastem公司签订协议,获得该药在俄罗斯、独联体、土耳其、中东、非洲的开发和商业化权利。
Ukoniq是一种口服、每日一次的PI3Kδ和CK1ε双效抑制剂,CK1ε是致癌蛋白翻译的调节因子,参与包括淋巴恶性肿瘤在内的癌细胞的发生和发展。已获批的PI3Kδ抑制剂大多会产生与自身免疫介导的相关毒性,如肝、肺毒性等,而Umbralisib的特异性优于当前的PI3Kδ抑制剂,且不会对PI3γ产生抑制。2021年2月,FDA批准用于治疗之前至少接受过一种基于抗CD20治疗方案的复发或难治性MZL成人患者,以及之前至少接受过三线全身治疗的复发或难治性FL成人患者。
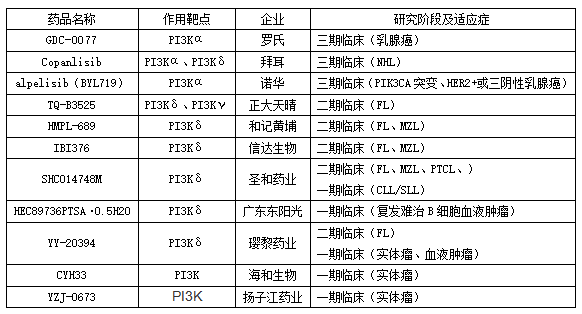
目前,我国还未有任何一款PI3K抑制剂获批上市,多款进口PI3K抑制剂处于三期临床阶段。此外,据insight数据库,国内已有多家企业开始布局该领域,如正大天晴、信达生物和圣和药业等,但国产PI3K抑制剂大多处于二期临床试验阶段。其中信达生物的IBI376(parsaclisib)是从Incyte Pharma公司授权引进的,而且今年2月,恒瑞医药与璎黎药业达成战略合作,以2000万美金的股权投资,获得后者PI3kδ抑制剂Linperlisib(简称YY-20394)在大中华地区的联合开发权益以及排他性独家商业化权益。
目前,我国PI3K抑制剂市场还是一片空白,期待早日有产品获批问世,造福广大患者。
声明:本文为作者独立观点,不代表贝壳社公众号立场,仅做分享交流。如需转载,请留言。




文章评论(0)