基因疗法,从不缺新技术
作者丨白头翁
●具有高转导效率,能感染分裂和非分裂的细胞;
●能靶向特定的细胞,且可以长期稳定表达转基因;
●具有较低的免疫原性或致病性,不会引起炎症;
●具备可大规模生产的能力。
然而,病毒载体还存在着诸如插入诱变、致癌,免疫反应和炎症加剧的等等风险。此外,病毒载体的大规模生产存在较高的技术壁垒。
过去基于病毒载体的基因疗法也曾发生过一系列的失败甚至死亡事件,其中最著名的就是1999年美国一位患有严重遗传病鸟氨酸转氨甲酰酶缺乏症的18岁少年Jesse Gelsinger,在接受宾夕法尼亚大学人类基因治疗研究所所长Jim Wilson教授主导的腺病毒基因治疗临床实验后,因为严重免疫反应导致多器官衰竭死亡,成为第一个因基因疗法而死的人。
今年1月国际顶级学术期刊《Science》发文报道直指基因治疗中所用的AAV病毒有致癌的可能。近期更是有Audentes公司研发的AT132基因产品在短短四个月内,发生了连续3起死亡事件,让我们不得不停下脚步,冷静思考基因疗法所存在的问题。
病毒载体的缺点,在某种程度上促进了非病毒载体的发展。常见的非病毒载体主要通过物理和化学方法来转导治疗性遗传物质,包括针,基因枪,电穿孔,声孔效应,光致成像,磁场转换,加氢,机械按摩,脂质体,磷酸钙,二氧化硅和纳米粒子等。
非病毒载体具有成本低、制备简单、便于大规模生产、安全性高、外源基因长度不受限制等优点,但同时也有明显的缺点,比如转染效率不理想及外源基因转导到宿主细胞后表达时间短等。
贝壳社整理了以下几款基于非病毒载体的基因疗法产品,从中可以看出非病毒载体的优势与不足,供大家参考和了解。
Vaxess Technologies正在开发一种可以采用MIMIX系统的SARS-CoV-2疫苗,MIMIX系统是一种储存稳定的单剂量皮肤贴剂,可以极大地改善疫苗管理。虽然其他制剂需要多次注射,但Vaxess疫苗与MIMIX系统的组合只需使用一次,而且皮肤贴剂操作非常简单,可以在家中使用。
其中,MIMIX使用丝蛋白纤维蛋白来稳定抗原分子,从而使疫苗能够在室温下存储和运输。 可以对纤维蛋白进行“调节”,以控制疫苗扩散到体内的速度。
MIMIX贴片敷用五分钟,可以将几十个丝制尖端嵌入皮肤。移除后,尖端留在皮肤中,在几周的时间里,它们逐渐将抗原制剂释放到体内。
当一种病毒感染人体时,一种强有力的免疫反应会在两到三周内分阶段发展。当病毒复制时,抗原被运送到淋巴结,在那里相应的T细胞和B细胞被激活。相比之下,人体在一两天内清除了大部分死亡病毒或蛋白质疫苗。
Vaxess的联合创始人兼CEO Michael Schrader解释说:“我们的系统是利用持续释放来欺骗免疫系统,使他们认为体内确实存在感染,而获得高质量和大量的抗体和T细胞。通过间隔细胞摄取,用贴片代替药丸,我们可以潜在地减少细胞死亡的数量。这是一种完美的复合效应,可以产生更强有力的免疫反应,并改善患者体验。”
今年7月,Sherlock宣布了与Binx Health的合作伙伴关系,他将把Sherlock的CRISPR技术与Binx io平台相结合,能够同时测试多达24个样本。
该测试将在各种CLIA豁免的环境中进行,包括药房,门诊和辅助生活设施。Sherlock联合创始人兼CEO Dhanda指出:“我们已经确定最大的需求领域之一实际上就是分散测试。可以给那些不能去医院的人或那些不愿意去的人提供选择。”
Sherlock还设想了可以在家里进行的简单,无仪器的测试,例如妊娠测试。该测试使用了Sherlock的INSPECTR技术,同时结合了仅在SARS-CoV-2 病毒存在时才被激活的合成生物学传感器。
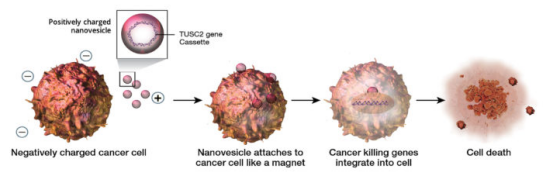
Genprex是一家临床阶段的基因治疗公司,通过Oncoprex纳米粒子输送平台将带有TUSC2的质粒包裹在设计成带正电荷的脂质纳米颗粒中送至细胞体内。这些纳米颗粒由表面活性剂和胆固醇组成。DOTAP(强阳离子)与胆固醇(电荷中性)的结合产生了一种非常稳定、持久的颗粒,因为纳米粒子本身带正电而被带负电的癌细胞吸引,纳米粒子通过与细胞膜融合,将它们携带的核酸释放到癌细胞中,重新编程癌细胞使其死亡。
Genprex创始人兼CEO Rodney Varner表示:“肿瘤活检显示,癌细胞摄取非病毒纳米粒子的速度是正常细胞的10至25倍。我们已经用这种系统治疗了50多名患者,由此显示出其良好的安全性。同时它还具有免疫刺激作用。”
TUSC2疗法被称为GPX-001。根据临床前数据,它与靶向治疗和免疫治疗都有协同作用。Genprex最近获得了FDA对GPX-001联合Tagrisso (osimertinib)的快速认证,这是阿斯利康针对由表皮生长因子受体(EGFR)突变驱动的非小细胞肺癌的靶向治疗。GPX-001与Tagrisso的Ⅰ期/Ⅱ期试验预计将于2021年初开始。该公司还启动了GPX-001与默克公司的免疫治疗药物Keytruda (pembrolizumab)联合的Ⅰ期/Ⅱ期试验。
Suono的首席运营官Carl Schoellhammer博士表示:“大多数人都熟悉用于成像的超声,如果你以比成像更低的频率使用超声波,则可以实现递送。”迄今为止,Suono的重点一直在胃肠道,可提供治疗炎症性肠病的药物。
首先,将含有活性分子的液体引入结肠。超声波会在液体中产生微小的气泡,然后气泡破裂,产生足以使药物穿过细胞膜的强力射流。整个过程耗时不到一分钟,与目前的炎症性肠病治疗相比,是一个巨大的进步,同时避免患者忍受在等待药物吸收时数小时的灌肠。
Suono除了提供抗炎小分子药物外,还使用超声波技术来传递小干扰RNA(siRNA),从而阻止肿瘤坏死因子TNF-α的产生。Schoellhammer强调:“这是一个完全裸露的RNA,没有脂质,什么都没有。”当科学家向患有结肠炎的小鼠递送RNA时,TNF-α的水平显着下降,从而抑制了炎症。用非常低的剂量(不到100 ng的RNA)即可获得结果,表明该疗法可以扩大用于人类。
传统的细胞疗法是将DNA插入T细胞,然后进行大量培养,最终再将修饰后的T细胞注入病人体内。对于癌症患者来说,这一治疗过程是比较漫长的。
为了加速这一过程,为癌症患者节省大量的时间,基于细胞生物学家已经使用电穿孔技术将DNA或RNA输送到细胞中的前例。Kytopen开发的一个新系统Flowfect,通过该系统可保持细胞持续流动,减少细胞暴露在电场中的时间,并立即将细胞输送到回收介质中。
Kytopen联合创始人兼CEO Paulo A. Garcia博士指出:“通过使用Flowfect系统的电能,我们可以将能量输送到细胞核,但仍能维持细胞活力和细胞功能。CAR T细胞疗法需要大约1亿个CAR -T细胞。我们可以以每分钟10亿个细胞的速度处理细胞。”
麻省理工学院机械工程副教授Cullen R. Buie是Flowfect技术的发明者之一,也是Kytopen的创始人之一,他说:“许多系统都有这样或那样的局限性。通常,一般都会涉及细胞健康、吞吐量和向细胞核传递的权衡。Flowfect系统提供了我们认为是所有这些因素的最佳组合。”
Kytopen已经转染了一系列细胞类型,包括活化和未活化的T细胞、单核细胞、巨噬细胞和诱导多能干细胞。此外,干细胞在转染后可以保持分化成不同谱系的能力。
从整体来看,非病毒载体具有低免疫原型、低成本、易规模化等优点,因而具有更好的临床应用前景,但还存在较多未解决的问题,如转染效率、细胞毒性、靶向性等,因此当前大部分细胞和基因疗法项目所采用的载体都为病毒载体,使用非病毒载体的项目大约仅占项目总数的36.6%。




文章评论(0)