仿制药,市场巨大,挑战严峻,路径清晰
目前我国制药企业中大部分以仿制药为主,药品也是仿制药占主流。数据统计显示,2020年,国内医药市场中,仿制药占比高达63%。受政策驱动、原研药专利相继期等因素的影响,我国仿制药行业市场规模不断增长,当年市场规模已达1077亿美元。有近5000家药企,已有药品批准文号总数达18.9万个,仿制药在处方量中占比达95%。
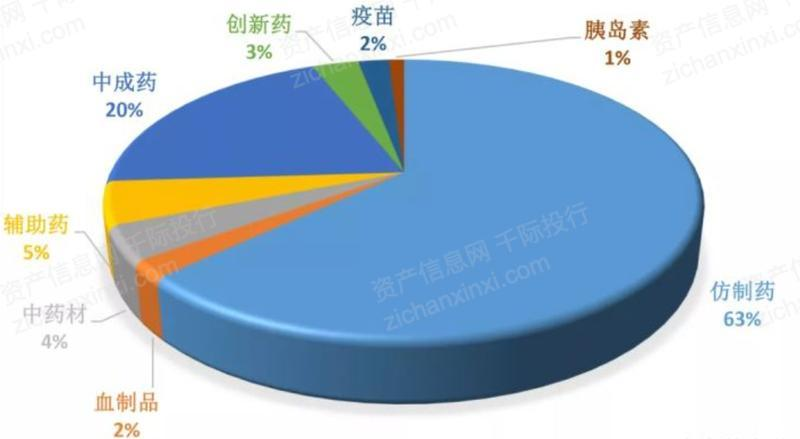
中国医药结构占比
来源:资产信息网 千际投行 中商产业研究院
经数据测算,2019年中国仿制药市场规模约为9707亿元,同比增长3.9%。2020受新冠病毒疫情影响,整体经济受到重创,药品市场也出现了罕见下滑,仿制药整体市场规模跌至8087亿元,同比下降16.7%。但随着疫情的控制和经济的恢复,预计2023年中国仿制药市场规模将回升至9349亿元。
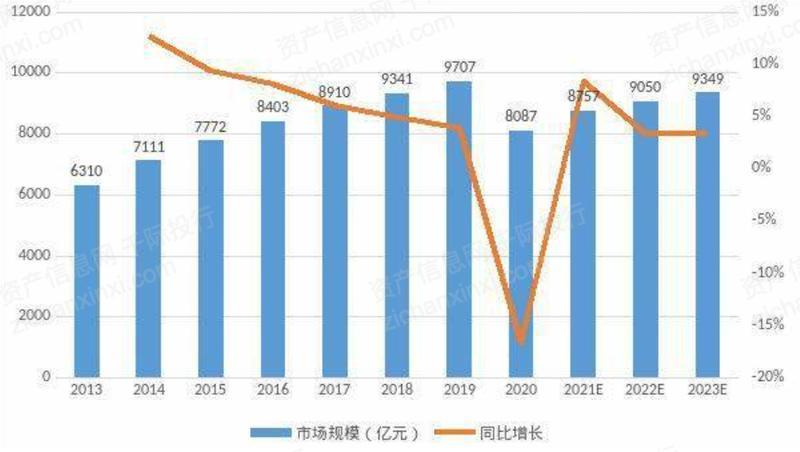
我国仿制药市场规模及增速
来源:资产信息网、千际投行、搜狐
市场回暖的同时,仿制药市场竞争将日趋激烈。
此外技术审评要求的技术门槛过低,仿制药审批权力不透明且过于集中,致使国内制药企业几乎不需进行深入研究即可达标。在此情况下,中国的一些仿制药目前能够做到的仅是化学等同,而生物等同、安全等同、临床等同还差得很远。
不能满足市场需求
药企研发投入不够,生产过程中的低水平重复问题很多,尤其是不能满足市场对于高质量仿制药品的大量需求。
另一方面,随着仿制药行业的快速发展,医药新时代已经到来,普通仿制药高价和高利润的时代已经过去了,药品利润将会大幅降低。在此情况下,一些药企可能更多地会选择市场价值和利润较高的高端仿制药,而抛弃普通仿制药。对此需要加强政策引导和出台相关激励和优惠政策。
同时,我国人口基数庞大,导致罕见病用药需求是发达国家的近百倍之多,而涉及罕见病的仿制药生产还比较少,一些药品的生产跟不上需求,而对于规模化生产的药企来说,需要投入较多成本才能生产此类药品,因此需要国家在政策层面予以扶持,激发企业的生产积极性。
另一个更为重要的原因是,由于我国公立医院在医药销售市场占据主导地位,而且各大医院普遍存在“以药补药”的现象,这两个因素直接导致医院享有合法销售药品的权利。由此产生的结果就是,医生不愿意开便宜的仿制药,病人也无法得到便宜的仿制药。
仿制药与普通山寨制药的不同之处在于,即便是仿制药,也是一个资本密集聚集的产业。因为从制药的生产流程看,首先需要通过化工原料的化学反应,制备出“医药中间体”,并从中得到有效成分,称为“原料药”,此外还要加入“药品辅料”,做成真正的胶囊、药片、注射剂。而所有这一切,需要一条完整的产业链才能完成。
因此也就决定了,只有作为行业龙头的大型企业,才能具备研发和生产能力。目前我国具有此能力的企业仍在少数。
随着我国人口老龄化的加速到来、越来越多的重磅创新药专利到期,人民对仿制药、尤其是慢性病仿制药的需求有增无减,预计未来我国仿制药市场将维持低速增长。
早在2016年3月,原国家食品药品监督管理局发布《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》,标志着仿制药一致性评价工作的正式开展,同时也标志着中国政府整顿仿制药行业的工作正式拉开序幕。
一致性评价的推进,是我国药品质量安全水平保障与行业标准统一规范的有力举措,它将促进产业集中度的提高。通过这项政策,仿制药将获得多方面的政策鼓励,包括在招标采购中可与原研药同组竞争,加速替代原研,无法通过一致性评价的品种可能会逐步退出市场。
通过完善医保支付标准和药品招标采购机制,支持优质仿制药研发和使用,促进仿制药替代,不断完善的行业政策有利于提高行业标准与药品质量安全水平,为优质制药企业创造了健康、良好的环境与体制保障。
2021年,国家卫健委、科技部等六部门近日联合印发通知,公布《第二批鼓励仿制药品目录》,其中包含阿福特罗、奥贝胆酸等17种药品。其实早在2019年,国家卫健委就发布了《关于印发第一批鼓励仿制药品目录的通知》,支持仿制药行业的发展。其中涵盖了多种抗癌药、罕见病药物以及此前曾出现短缺的药品等。侧面说明中国罕见病带来的仿制药市场开发空间较大。在罕见病仿制药方面,药企或可以根据自身能力开拓新蓝海。

第二批鼓励仿制药品目录
来源:国家卫健委
另外,中国药企要想成为世界级制药企业,不但要走出去,而且要转型升级,要仿创结合,做创新制剂,是投入最少、也是最便捷的发展路径。仿制药企业除了往创新药方向发展,还可以根据自身基础成为CDMO,整合自身优势,多点开花,打开局面。
另外,出海方面也有好消息。不只在国内,除了大家熟知的美国、欧盟、日本等大市场,在一些新兴市场(如中东、北非、撒哈拉以南非洲、拉美、俄罗斯等),对仿制药及创新药的需求正在增加,也为中国药企仿制药“出海”带来新的机会。先声药业便在布局出海。其在致力于与跨国药企合作的同时,通过专利授权、海外商业化等方式,推动自研、自有创新药的出海。目前先声药业已经在美国、欧洲等国家和地区成立了具有一定规模的BD团队,年度评估项目数百个,国际业务部已经完成了多个制剂、原料药产品在美国、欧洲、“一带一路”沿线国家的海外出口。
在转型CDMO方面,有药企则依靠“仿制药+创新药+CDMO”打开格局。百诚医药——仿制药CRO市场龙头便是其中之一。百诚医药在持续深耕仿制药 CRO技术平台的基础上,强化CDMO业务和研发创新平台布局,将持续受益于仿制药CRO“业务收入高增长+收入分成贡献”、以及自主研发仿制药和创新药权益转让的收益,和CDMO业务带来的业务闭环,整体业绩继续呈现高速增长。
企业存在的最大价值是为社会解决问题。只要顺应市场需求,为大众解决医药健康问题,不断扩大优势,随市场之机适时应变,都将打出新蓝海。
参考资料:
1.《竞争日趋激烈,仿制药企如何转型升级?》,研发客,2019.
2. 《2022年仿制药行业研究报告》,千际指数,2022-08-15.
3.《中国仿制药行业发展任重道远》,热点我见,2021-10-30.
4.《刚刚,国家卫健委发文,这些仿制药机会来了(附名单)》,赛柏蓝,2019-10-11.


文章评论(0)