Padcev即将落地中国,ADC靶点新星Nectin-4在悄悄拔尖
ADC强大的疗效与截然相反的低毒副作用也成为了这个时代抗癌领域新的研究热点。ADC药物中较为热门靶点包括HER2、EGFR、CLDN18.2、TROP2、c-Met、CD19、PSMA、Muc1、BCMA和PDL1,且大多数是已被市场验证的成熟靶点。
Nectin-4靶点是ADC的新星靶点,与HER2、EGFR、Trop2等热门靶点相比,目前针对Nectin-4靶点布局的产品较少,且全球只有一款ADC产品Padcev上市,未来留给药企们开发空间较大。
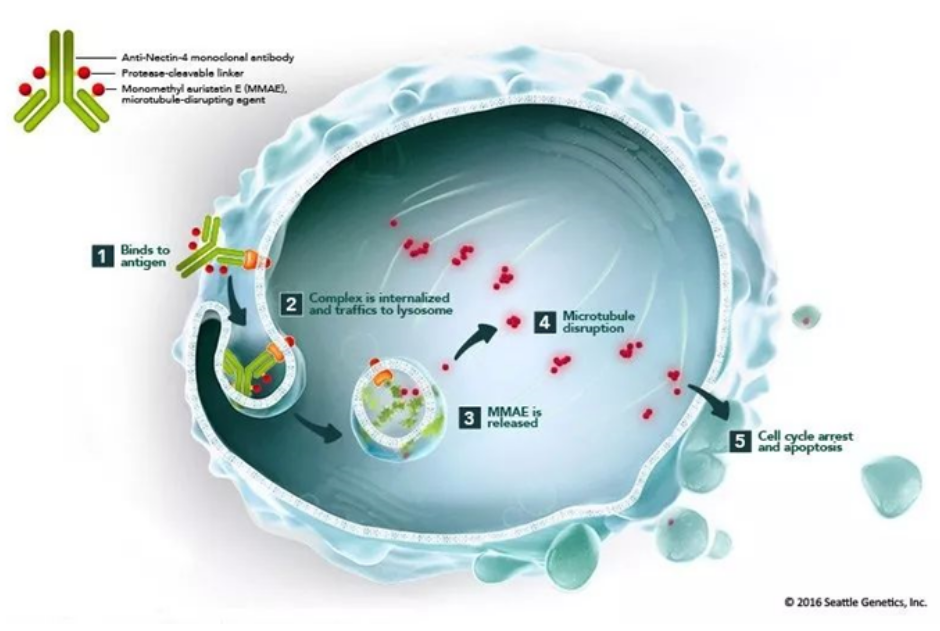
Padcev作用机制
来源:Seagen官网
2019年12月,FDA批准了Padcev用于治疗既往在手术前(新辅助)或手术后(辅助)、局部晚期或转移性背景下接受过PD-1或PD-L1抑制剂和含铂化疗的局部晚期或转移性尿路上皮癌的成人患者。
2021年7月,FDA授予Padcev在美国的常规性获批,且同时依据II期临床试验EV-201 cohort 2的结果,扩展了适应症,用于不适宜顺铂治疗但曾受过PD-1/PD-L1抑制剂治疗的局部晚期或转移性尿路上皮癌患者。临床数据显示,Padcev治疗迅速缩小了大多数患者的肿瘤,客观缓解率(ORR)为44%,完全缓解率为(CR)12%,中位缓解持续时间(DoR)为7.6个月。
2022年12月,Padcev联合Keytruda治疗不适合接受含顺铂化疗的局部晚期或转移性尿路上皮癌的sBLA获FDA受理。Padcev联合免疫治疗或将成为尿路上皮癌患者治疗的新方向,为顺铂不耐受的晚期尿路上皮癌患者提供了新的治疗选择。研究指出,Padcev+Keytruda有效率高达73.3%,1年总生存(OS)率为81.6%。
此次Padcev在中国的上市申请基于一项单臂、开放标签、多中心的 II 期临床试验EV-203试验(NCT04995419)的数据。
该试验旨在评估Padcev治疗既往接受PD-1/PD-L1抑制剂和含铂化疗治疗的局部晚期或转移性尿路上皮癌的中国患者的疗效、安全性和药代动力学特征。
结果显示,EV-203达到了其主要终点,即与历史对照相比,经独立审查委员(IRC)确认的接受Padcev单药治疗患者的客观缓解率(ORR)达到统计学意义,该研究的有效性和药代动力学数据与全球数据一致。
目前,Padcev已在美国、日本以及欧洲等主流国家上市,而国内Nectin-4 ADC靶向药物市场依旧空白。如果Padcev顺利获批,将有望填补空白,开辟中国Nectin-4 ADC靶向药物新时代。
Nectin-4是一种Ⅰ型膜蛋白,在正常的胚胎和胎儿组织中含量很高,在成人健康组织中表达量很低,但在多种肿瘤细胞中高表达,如尿路上皮癌、膀胱癌、乳腺癌、卵巢癌、胃癌、肝细胞癌和胰腺癌,而且,Nectin-4与肿瘤的发生和转移具有密切的关系,可通过激活PI3K/AKT途径促进肿瘤细胞增殖、分化、迁移、侵袭等。
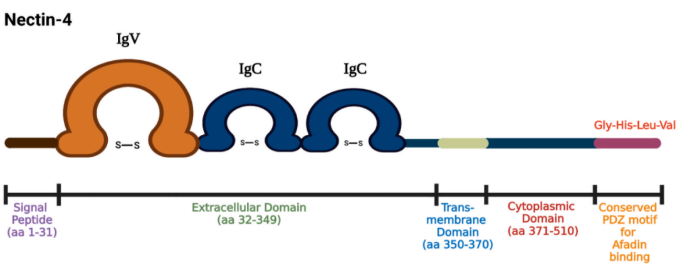
Nectin-4 结构
来源:Nature Drug Discovery
Nectin-4是免疫球蛋白超家族中nectin家族的成员,目前nectin-4相关药物开发的主要聚焦于晚期尿路上皮癌。
研究显示,60%膀胱癌样本和34%上尿路尿路上皮癌样本可见中高水平nectin-4蛋白表达。在上尿路尿路上皮癌中,nectin-4蛋白高表达与疾病进展明显升高(P=0.03)和癌症特异性死亡率(P=0.04)相关,并且nectin-4是高危患者疾病进展的独立预测因子(HR=3.32,P=0.03)。
根据东亚前海证券数据,2020年,全球新增尿路上皮癌病例51.6万例,其中,中国新增约约7.7万例。预计到2025年,全球新增尿路上皮癌病例数将达到58.6万例,中国约9.1万例。因此nectin-4已成为一个极具前景的治疗靶点。
根据Seagen财报,2022年Padcev的全球销售额为7.54亿美元,同比增长40%,作为全球首个获批治疗局部晚期或转移性尿路上皮癌的ADC药物,销售额有望在2023年突破10亿美元大关,并继续保持稳定的发展态势,在Nature Reviews Drug Discovery期刊上发表的分析文章中预测,到2026年Padcev销售额预计将达到35亿美元,Padcev被认为是未来的“DS-8201”。此次Padcev进军中国,正是其拓展全球市场的一个大重要举措。
Padcev的成功及nectin-4 ADC的市场趋于空白,目前越来越多的药企开始对nectin-4 靶点投来欣赏的目光,入局者逐渐增多,特别是中国的Biotech,参与的热情不断高涨。聚焦国内,目前迈威生物研发进度靠前,百奥泰生物、石药集团紧随其后,此外,君实生物也开始布局该靶点。
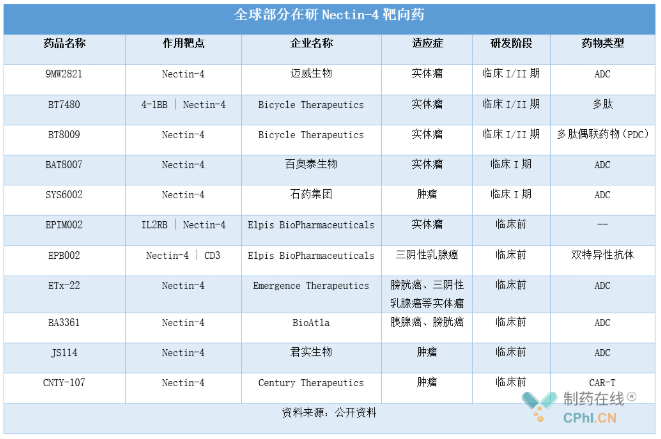
全球部分在研Nectin-4靶向药
来源:CPHI制药在线
迈威生物的9MW2821是是国内首个进入临床的Nectin-4靶向ADC创新药。9MW2821具有组分均一、纯度较高、便于产业化的优点,在亲和力、内吞性质、初步的体内及体外药效活性、药物代谢性质、初步安全性等方面均显示其具有良好的成药性。
临床前药理毒理结果显示,9MW2821在多种动物肿瘤模型中均具有良好的抑瘤效果,在食蟹猴、小鼠体内的安全性显示具有更好的治疗窗口。9MW2821于2021年10月获CDE批准IND,可针对包括尿路上皮癌、乳腺癌、肺癌等多个实体瘤开展临床研究,2022年8月,9MW2821还获得了美国FDA批准临床,用于治疗实体瘤,目前正在国内多家医院开展I/II期临床研究。
百奥泰生物的BAT8007由重组人源化抗Nectin-4抗体与毒性小分子拓扑异构酶I抑制剂通过公司自主研发的可剪切连接子连接而成。临床前研究显示BAT8007具有高效的抗肿瘤活性,毒素小分子有较强的旁观者效应,可望有效克服肿瘤组织的异质性。同时,BAT8007还表现出较好的稳定性及安全性,血浆中释放的毒素小分子极低,预示了脱靶毒性风险的降低,目前处于临床I期。
石药集团的SYS6002是采用石药专有的酶催化定点抗体偶联技术,能将有效的有丝分裂抑制剂MMAE针对性地导向Nectin-4表达的癌细胞,而其连接子的稳定性有助于将高浓度的MMAE送达肿瘤中,并同时通过减少不良的全身暴露量而将副作用减低,目前处于临床I期。
目前,国内在研的nectin-4 ADC产品都处于临床早期,但是值得关注的是,前不久石药集团成功将尚处于临床早期的SYS6002以高达7亿的总金额出海,以及此次Padcev打入中国市场,都在证明Nectin-4靶点的在悄悄掘起。
纵观nectin-4 ADC赛道,目前尚不拥挤,入局者不多,相对宽松的竞争环境给了药企们更多的时间和精力投入研发,那么谁能领跑成为国产nectin-4 ADC市场的开局者?相信时间会给出答案的。
参考资料:
1、《ADC爆发的下一步--思考如何将商业价值最大化?且看五款明星ADC生命周期管理办法》猎人俱乐部,2023年3月3日
2、《安斯泰来/Seagen Nectin-4 ADC在华申报上市!》求实药社,2023年3月11日
3、《一文探讨:新型靶点nectin-4的研究现状和未来》医脉通泌尿外科,2022年1月30日
4、《新药 | Nectin-4:实体瘤治疗潜力靶点,Padcev表现亮眼,石药集团等国内药企积极布局》CPHI制药在线,2023年2月14日


文章评论(0)