在过去的一个月里,国内药企共发生8起License in交易及2起License out交易(数量较2月份统计的8起有所上升),交易总金额超百亿,其中29日发生的3起License in交易总金额超30亿。此外,10起交易金额均达上千万元,其中,思路迪医药引进的CD47单克隆抗体IMC-002费用高达32.8亿元。
进一步梳理可发现,所有药企中,联拓生物共引进2款产品,而海思科既有产品引进又有产品出海;所有引进产品主要覆盖抗病毒、胃食管反流、淋巴瘤、实体瘤、胶质母细胞瘤等肿瘤疾病领域,且均具有明显治疗优势。
贝壳社现根据公开资料及各公司官网信息将3月份国内药企License in /out 交易项目(不完全)整理如下,供大家参考。
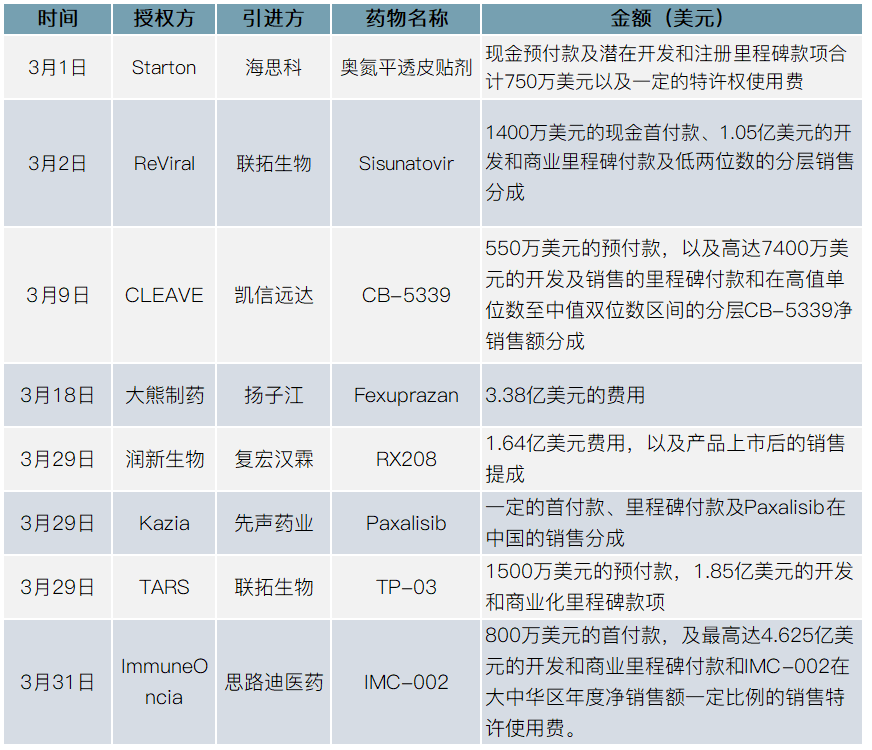
2021年3月License in交易汇总
(贝壳社制图)
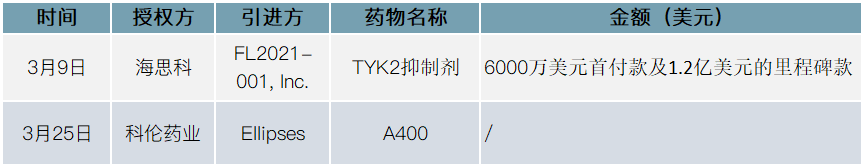
2021年3月License out交易汇总
(贝壳社制图)
3月1日,海思科医药集团股份有限公司(海思科)与Starton Therapeutics Inc.(Starton)签订了关于奥氮平透皮贴剂(STAR-OLZ)的合作协议,海思科获得在中国大陆区域开发、注册和商业化STAR-OLZ的独家权利。根据协议,海思科需向Starton支付包括现金预付款及潜在开发和注册里程碑款项合计750万美元。此外,Starton还有可能获得一定的特许权使用费。
据悉,STAR-OLZ可通过每周一次透皮给药,拟用于治疗由化疗引起的恶心、呕吐(CINV)和PARP抑制剂引起的恶心、呕吐(PIINV)。通过研究发现,STAR-OLZ对皮肤具有良好的耐受性且易于去除,并且与ZYPREXA(奥氮平片)相比,具有较低的副作用。
3月2日,联拓生物与临床阶段生物制药公司ReViral达成独家合作和许可协议,联拓生物将在中国大陆、香港、澳门和新加坡地区开发和商业化Sisunatovir。根据协议,联拓生物需向ReViral支付 1400万美元的现金首付款,以及高达1.05亿美元的开发和商业里程碑付款。此外,ReViral将在许可地区售出药物的净销售额中可获得低两位数的分层销售分成。
据悉,Sisunatovir是一种口服融合抑制剂,旨在通过抑制由F介导的病毒与宿主细胞的融合,以阻断呼吸道合胞病毒(RSV)复制。FDA已经授予Sisunatovir快速审核通道资格。近期,ReViral正式启动Sisunatovir针对儿童和高危成人患者的两项国际多中心2期临床研究。
3月9日,凯信远达与临床阶段的生物制药公司CLEAVE签订独家许可协议,凯信远达获得CLEAVE全球首创新药 VCP/P97抑制剂CB-5339大中华区许可权益。根据协议,凯信远达需向CLEAVE 支付550万美元的预付款,以及高达7400万美元的开发及销售里程碑付款和在高值单位数至中值双位数区间的分层CB-5339净销售额分成。
据悉,CB-5339是一款口服二代小分子VCP/p97抑制剂,CLEAVE正在推进其用于急性髓性白血病(AML)和骨髓增生异常综合症(MDS)的1期临床研究。与此同时,美国国家癌症研究所(NCI)也将开展1期临床试验以评估其在实体瘤和淋巴瘤中的应用。
3月18日,扬子江药业集团(扬子江)通过子公司上海海尼药业与韩国生物制药公司Daewoong Pharmaceutical(大熊制药)达成战略合作。海尼药业可获得治疗胃食管反流病药物Fexuprazan在大中华地区的研发、销售和供应权益。根据协议,海尼药业需向大熊制药最高支付3.38亿美元的费用。
据悉,Fexuprazan是大熊制药自主研发的一款新型钾离子竞争性酸阻滞剂(P-CAB),属于新一代质子泵抑制剂(PPI),通过可逆地阻断分泌胃酸的质子泵,治疗胃食管反流病。2020年5月,大熊制药公布了Fexuprazan在韩国进行的3期临床结果,数据显示糜烂性食管炎患者在接受Fexuprazan治疗的第8周显示出99%的治疗率。目前,Fexuprazan在国内正在开展3期临床试验。
3月29日,复宏汉霖与润新生物科技有限公司(润新生物)达成一项独家许可合作,复宏汉霖获得BRAF V600E抑制剂RX208在中国(包括香港、澳门和台湾地区)进行研究、开发、生产和商业化等的独家权利。复宏汉霖需向润新生物支付1.64亿美元费用,以及产品上市后的销售提成。
据悉,RX208是一款针对BRAF V600E突变的选择性小分子抑制剂,临床上拟用于治疗BRAF V600E突变阳性、不适合手术的局部晚期或转移性恶性实体瘤。临床前研究结果表明,RX208具有显著的肿瘤抑制活性及良好的安全性。目前处于临床1期,早期临床研究也展现出初步疗效,且副作用低,RX208有望成为Best-in-Class的BRAF V600E小分子抑制剂。
3月29日 ,先声药业集团有限公司(先声药业)附属公司与澳大利亚肿瘤药物开发公司Kazia Therapeutics(Kazia)签署独家许可协议,先声药业获得Paxalisib在大中华地区(中国大陆,香港,澳门和台湾)所有适应症的开发和商业化的权益。根据协议,先声药业需向Kazia支付一定的首付款、里程碑付款及Paxalisib在中国的销售分成。
据悉,Paxalisib是一款具有高效血脑屏障穿透性的PI3K/mTOR通路抑制剂,目前正在开展全球2/3期的GBM AGILE胶质母细胞瘤平台临床试验。临床2期研究的中期数据显示,Paxalisib用于MGMT非甲基化的新发胶质母细胞瘤(GBM)患者,可显著提升中位生存期(mOS)和中位无进展生存期(mPFS)。
3月29日,联拓生物与临床后期阶段的生物制药公司Tarsus Pharmaceuticals,Inc.(TARS)达成战略合作,联拓生物获得在大中华区开发和商业化TP-03的专有权。根据协议,联拓生物需向TARS支付1500万美元的预付款,1.85亿美元的开发和商业化里程碑款项,包括到2021年6月30日的1000万美元,以及在未来12个月内有望获得的近期临床里程碑的4500万美元。
据悉,TP-03是一种新型的研究性治疗药物,旨在靶向和根除蠕形螨。它是昆虫和蛛网膜GABA-Cl通道和高度亲脂性分子的有效、非竞争性拮抗剂,可促进其在螨虫所在的毛囊的油性皮脂中摄取。TP-03针对蠕形螨睑缘炎已经完成四项2期临床试验,且均达到各自终点。
授权方:ImmuneOncia
引进方:思路迪医药
3月31日,思路迪医药与ImmuneOncia Therapeutics(ImmuneOncia)达成合作协议,思路迪医药获得新一代抗CD47单克隆抗体IMC-002肿瘤适应症在大中华区(中国大陆、香港、澳门和台湾地区)的开发、生产和商业化的独家授权。根据协议,思路迪医药需向ImmuneOncia支付800万美元的首付款,及最高达4.625亿美元的开发和商业里程碑付款和IMC-002在大中华区年度净销售额一定比例的销售特许权使用费。
据悉,IMC-002是一款全人源化IgG4单克隆抗体新药,它通过阻断CD47-SIRPα相互作用,促进巨噬细胞对肿瘤细胞的吞噬作用。现有临床前数据显示,IMC-002与人CD47亲和力强,可以最大限度地提高疗效,而不会出现与红细胞结合或引起贫血等其他在研CD47抑制剂常见的副作用。目前,该药物处于全球1期临床开发阶段。
授权方:海思科
引进方:FL2021-001, Inc.
3月9日,海思科医药集团股份有限公司(海思科)控股子公司 FronThera International Group Limited(FT集团)与 FL2021-001, Inc.签署股权转让协议,FL2021-001, Inc.由此获得FT集团TYK2抑制剂所有权。而FT集团可获得最高合计1.8亿美元的转让款,其中包含6000万美元首付款及1.2亿美元的里程碑款。
据悉,TYK2属于口服选择性酪氨酸激酶2(TYK2)抑制剂,是一种介导免疫信号的非受体酪氨酸激酶,可介导IL-23、 IL-12和I型干扰素驱动的信号通路。其中,TYK2信号参与多种免疫相关疾病的的病理生理过程,如银屑病、狼疮和炎症性肠炎等,目前全球尚未有TYK2抑制剂获批上市。
3月25日,四川科伦药业股份有限公司(科伦药业)宣布其控股子公司四川科伦博泰生物医药股份有限公司(科伦博泰)与英国Ellipses Pharma LTD(Ellipses)达成区域授权合作协议。Ellipses获得科伦博泰创新小分子肿瘤靶向RET激酶抑制剂项目(A400)欧美等区域独家授权。科伦博泰保留大中华区及韩国、新加 坡、马来西亚等部分亚太地区的权利,双方将在各自区域内进行开发、商业化等活动,并利用各自区域内数据支持该项目的全球研发。
据悉,A400是科伦博泰研发的具有自主知识产权的小分子选择性靶向RET激酶抑制剂,临床前研究表明A400具有良好的体内外激酶抑制活性和选择性,尤其在动物血/脑暴露量等方面具有优势;对临床已有报道的多种临床耐药突变有效,具有克服临床耐药突变和提高对脑转移癌临床疗效的潜力。2021年3月科伦博泰已向NMPA正式提交A400的IND申请。




文章评论(0)