冲击100亿欧元,赛诺菲度普利尤单抗再下一城

截图自NMPA
特应性皮炎(AD)是一种具有遗传倾向的慢性、复发性、炎症性皮肤病,患者常合并过敏性鼻炎、哮喘等其他特应性疾病,故被认为是一种系统性疾病。而目前国内针对中重度特应性皮炎的治疗药物十分有限,外用激素等局部疗法对中重度特应性皮炎患者疗效有限且难以长期使用,免疫抑制剂或口服糖皮质激素等系统性治疗方式有可能导致严重的副作用。
随着度普利尤单抗正式在国内获批上市,开始逐步改善大多数中重度特应性皮炎患者通过传统治疗后仍需面临“治疗失败”或“疾病控制不佳”的窘境。
由于国内缺乏针对AD的有效治疗方案,度普利尤单抗被纳入第二批临床急需境外新药名单,且基于该药物能快速、显著、持续地改善特应性皮炎患者的皮损程度和瘙痒症状,并有效改善患者的生活质量,2020年2月《中国特应性皮炎治疗指南》正式将度普利尤单抗纳入特应性皮炎的治疗推荐。
2020年6月,度普利尤单抗首次在中国获批上市,用于治疗外用处方药控制不佳或不建议使用外用处方药的成人中重度特应性皮炎,并成功进入医保目录;2021年9月,度普利尤单抗再次获批用于12岁及以上青少年及成人的中重度特应性皮炎。此外,其用于治疗外用处方药控制不佳或不建议使用外用处方药的≥6岁至<12岁儿童和成人中重度特应性皮炎患者的适应症已纳入优先审评。
作为唯一一款已上市的IL-4Rα全人源抗体,度普利尤单抗2020年销售额为40.45亿美元,且据赛诺菲公布的2021年上半年财报显示,该药物销售额已达26.82亿美元。不过,赛诺菲CEO Paul Hudson表示,与此前为度普利尤单抗设定的100亿欧元年销售额目标相比,目前该药物的发展“仍处于起步阶段”。
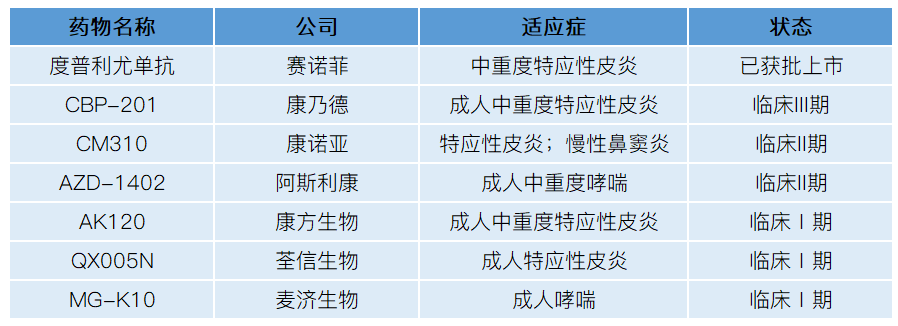
贝壳社制图
CBP-201是康乃德生物医药通过其特有的免疫调节技术平台自主开发的抗IL-4Rα抗体新药,主要用于治疗中重度特应性皮炎和其他多种重大未满足临床需求的Th2炎症性疾病。且1a临床研究结果表明,CBP-201具有良好的耐受性,并能够使得血清中胸腺激活和调节趋化因子(TARC/CCL17,Th2活性的生物标志物)持续快速降低。此外,与度普利尤单抗2周一次给药的模式相比,CBP-201有望实现更优的4周一次给药方式,提高患者用药依从性。
康诺亚的CM310是首个国产且获批临床的IL-4Rα抗体,有效治疗各种成人、青少年及儿童Ⅱ型过敏性疾病(重度特应性皮炎、中重度嗜酸性哮喘、慢性鼻窦炎拌鼻息肉)及潜在慢性阻塞性肺病。其治疗特应性皮炎的适应症已在国内进入临床II期,预计2023年将向NMPA递交NDA申请;治疗慢性鼻窦炎的适应症预计于2022年启动III期临床。
阿斯利康的AZD1402是一款吸入式IL-4α受体拮抗剂,可用于治疗中重度哮喘,临床结果显示AZD1402能显著降低IL-4信号通路的下游生物标志物水平,具有抑制IL-4介导的炎症反应的潜力。
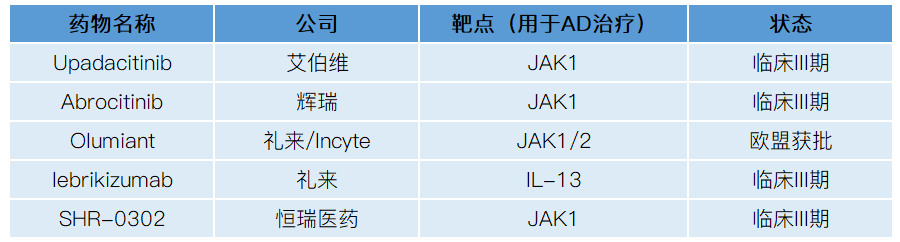
贝壳社制图
Upadacitinib(乌帕替尼)是艾伯维开发的一种口服,且具有选择性和可逆性JAK1抑制剂。2017年FDA正式批准Upadacitinib上市,用于对甲氨蝶呤反应不足或不耐受的中重度活动性类风湿关节炎成人患者。今年6月,艾伯维已在《柳叶刀》杂志发表了乌帕替尼针对中重度特应性皮炎的关键性全球III期临床研究的主要分析结果,数据显示,与安慰剂相比,乌帕替尼在成人和青少年中重度AD患者中表现出显著改善的皮损清除率和瘙痒减轻。
值得一提的是,乌帕替尼用于中重度AD已获FDA突破性疗法认定,并被NMPA纳入优先审评。
Abrocitinib是辉瑞研发的一种口服小分子高选择性JAK1抑制剂,据辉瑞公布的III期研究(JADE MONO-2)完整结果显示,与安慰剂相比,Abrocitinib在改善皮损清除、湿疹面积和严重程度、瘙痒方面均显示统计学上的显著优越性,达到全部共同主要终点和关键次要终点。该药物曾获得FDA授予用于治疗中度及重度AD的突破性药物资格。
Olumiant(Baricitinib)是由Incyte开发的一种JAK1/2酪氨酸激酶抑制剂,随后礼来通过与Incyte达成协议获得Baricitinib的全球独家合作权。该药物已获FDA批准,用于对TNF抑制剂疗法反应不足的中重度活动性类风湿性关节炎患者,且用于AD的适应症已在欧盟获批,是全球首个被批准治疗特应性皮炎的JAK抑制剂。
此外,礼来还通过收购收购Dermira,获得AD新药lebrikizumab的全球权益。其中,lebrikizumab是一款创新人源化抗IL-13单克隆抗体,研究表明,IL-13是介导特应性皮炎的关键因子,可促进2型炎症反应,从多方面驱动特应性皮炎的病理生理学。近日,礼来宣布 lebrikizumab作为单一疗法治疗成人和青少年患者中重度AD的两项III期临床试验(ADvocate1和ADvocate 2)已达到主要终点和全部次要终点,与度普利尤单抗相比,lebrikizumab疗效相似或更优,且具有给药便捷(两周或四周一次)、较低的结膜炎发生率优势。
SHR-0302是恒瑞医药开发的一种高选择性JAK1抑制剂,其用于AD的II期临床QUARTZ2研究中已获得积极结果,且总体耐受性良好。基于此,NMPA已授予SHR-0302用于AD的突破性疗法称号,此外,SHR0302还在国内开展了针对类风湿性关节炎、溃疡性结肠炎、克罗恩病等多项临床研究。


文章评论(0)