【12月7-10日】CIS-Asia2021|第十二届化学制药国际峰会-亚洲

举办时间丨2021年12月7-10日
举办地点丨中国 · 北京丰大国际大酒店
主办单位丨百世传媒|Best Media、中国药学会制药工程专业委员会
支持单位丨百世药学院、药方舟、苑东生物
合作媒体丨制药在线、药渡、药智网、中国生物器材网、贝壳社、生物探索、生命奥秘、肽度 TIMEDOO、化工仪器网、盖德化工网、来宝网、药源网、中美健康咨询网、86175、医谷网、中国化工制造网、会会药咖、网化商城、戊戌数据、Chemindustry、CBG资讯、中食药信息网、insight数据库、注册圈、杉树园、分析测试百科网、新药汇、药物递送、药鹿、仪器信息网、每日经济新闻
参会注册通道及展商参展通道即将关闭
期待与您相会北京
扫描下方二维码填写报名信息进行详细咨询
我们的工作人员将于24小时内和您联系
Part 1
赞助商

Part 2
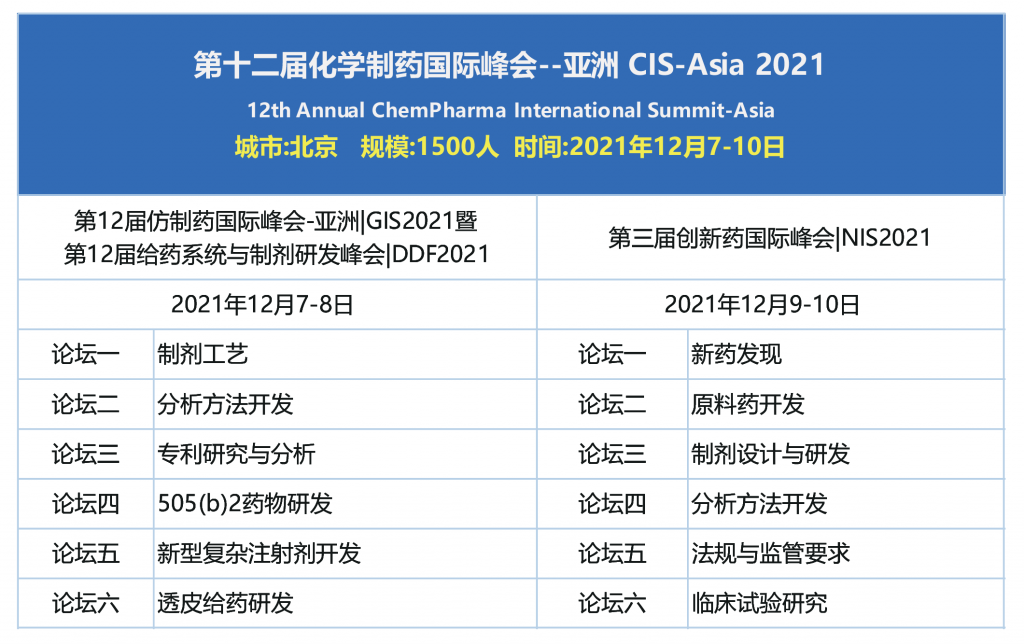
第12届仿制药国际峰会
第12届给药系统与制剂研发亚洲峰会
演讲嘉宾
Part 3
第三届创新药国际峰会
演讲嘉宾



Part 4
第12届仿制药国际峰会
第12届给药系统与制剂研发亚洲峰会
12月7-9日(周二~周三)
主办方致欢迎词
- 08:20 大会主持人致开幕词
俞雄,名誉主任委员,中国药学会制药工程专业委员会
- 08:30 新形势下药企如何构筑仿制药竞争壁垒
俞雄,名誉主任委员,中国药学会制药工程专业委员会
- 09:15 高端创新制剂的发展现状与挑战
张强,特邀教授,北京大学
10:00 茶歇
- 10:30 日本药物研发特色与实例初探
刘世成,副总经理,云鹏医药集团
- 11:15 圆桌讨论:仿制药VS创新药,国内药企未来如何选择?
刘万卉,副总裁,绿叶制药
刘世成,副总经理,云鹏医药集团
张强,特邀教授,北京大学
魏世峰,总经理,北京罗诺强施医药
叶英,董事长,力品药业(厦门)股份有限公司
12:05 午餐
12月7日(周二)
论坛主持:曹家祥,总裁及首席科学家,Abravit Biopharm公司
- 13:30 固体制剂连续制造系统的要点
曹家祥,总裁及首席科学家,Abravit Biopharm公司
- 14:30 中试及中试放大技术转移的计划和成功的要素
张津州,研发总监,华海药业
- 15:30 茶歇
- 16:00 制剂生产工艺放大可行性及技术转移要点
陈洪,副总经理,苑东生物
- 17:00 小组讨论:药物制剂技术国际化难点探讨
曹家祥,总裁及首席科学家,Abravit Biopharm公司
张津州,研发总监,华海药业
叶启丞, 中试负责人,苑东生物
- 17:45 会议结束
12月8日(周三)
论坛主持:吴正红,教授,中国药科大学
- 08:30 制剂处方工艺开发中的关键工艺点的确定
魏世峰,总经理,北京罗诺强施医药
- 10:00 结合CQA和CPP浅析放大工艺的选择(30m)
徐兵,副总经理,创志科技
10:30 茶歇
- 11:00 基于结构的高端制剂工艺剖析与质量评价
张继稳,研究员,中国科学院上海药物研究所
12:00 午餐
论坛主持:魏世峰,总经理,北京罗诺强施医药
- 13:00 制剂工艺验证中的过程控制和关键工艺参数的确认
吴正红,教授,中国药科大学
- 13:45 浅析制剂从实验室到临床历经的多重挑战
李三鸣,教授,沈阳药科大学
14:30 茶歇
- 15:00 物料属性对制剂产品生命周期的重要性
祁小乐,副教授,中国药科大学
-
15:45 小组讨论:研发后期转移到大生产阶段的成功与失败经验分享 程秀秀,资深顾问,国内外药企
魏世峰,总经理,北京罗诺强施医药
吴正红,教授,中国药科大学
- 16:30 会议结束
12月7日(周二)
论坛主持:严子梦,执行副总经理,北京鑫开元医药科技
- 13:30 杂质限度法妙用
陈洪,副总经理,苑东生物
- 14:30 样品制备自动化 —— 方法转移、验证与法规符合性(30m)
赵宇,业务发展总监,力扬企业有限公司
15:30 茶歇
- 16:00 质量体系对制药工业的作用
严子梦,执行副总经理,北京鑫开元医药科技
- 17:00 小组讨论:分析方法法规要求趋势分析
何威轩,国际部总经理,成都倍特药业
严子梦,执行副总经理,北京鑫开元医药科技
陈洪,副总经理,苑东生物
- 17:45 会议结束
12月8日(周三)
论坛主持:奚凤德,首席科学家,京新药业,前USP美国副总裁
- 08:30 怎样确认和验证溶剂残留方法
周立春,药典委员会委员,北京市药品检验鉴定研究所
- 09:30 溶出技术在药物研发及生产中的关键作用(30m)
陆家祺,技术总监,深圳市锐拓仪器设备有限公司
10:30 茶歇
- 11:00 如何衔接研发分析与商业生产QC实验室
田芸,副总经理,普霖贝利生物医药
12:00 午餐
论坛主持:张金兰,研究员,中国医学科学院药物研究所
- 13:00 药用辅料吐温分析新方法研究与应用
张金兰,研究员,中国医学科学院药物研究所
- 13:45 应用矩阵法进行杂质的风险评估
奚凤德,首席科学家,京新药业,前USP美国副总裁
14:30 茶歇
- 15:00 疑难分析问题解决的发散性思维—案例分享
刘国柱,分析技术总监,长沙晨辰医药科技
- 15:45 小组讨论:怎么做好方法耐用法验证?
奚凤德,首席科学家,京新药业
刘国柱,分析技术总监,长沙晨辰医药科技
张金兰,研究员,中国医学科学院药物研究所
- 16:30 会议结束
12月7日(周二)
论坛主持:程秀秀,资深顾问,国内外药企
- 13:30 美国仿制药专利挑战和首仿案例分析(45m)
程秀秀,资深顾问,国内外药企
- 14:30 药物专利授.确权程序实验数据的补充(30m)
胡洪慧,合伙人,万慧达知识产权
- 15:00 国内仿制药专利挑战策略(45m)
曹津燕,执行合伙人,北京瑞恒信达
- 15:30 茶歇
- 16:00 仿制药晶型专利无效案例分析
耿佳,知识产权总监,石药集团
- 17:00 小组讨论:如何绕开仿制药开发中的专利陷阱?
程秀秀,资深顾问,国内外药企
曹津燕,执行合伙人,北京瑞恒信达
耿佳,知识产权总监,石药集团
- 17:45 会议结束
12月8日(周三)
论坛主持:窦夏睿,知识产权总监,扬子江药业集团
- 08:30 专利法第四次修改后医药企业面临的机遇与挑战(40m)
张清奎,原部长,中国国家知识产权局医药生物发明审查部
- 09:10仿制药晶型开发与专利保护和突破(40m)
郝红勋,教授,天津大学
- 09:50 仿制药如何突破知识产权壁垒(国内企业案例分析)(40m)
孔祥生 ,总裁助理, 丽珠医药集团
10:30 茶歇
- 11:00 仿制药立项过程中的专利评估和规划
窦夏睿,知识产权总监,扬子江药业集团
12:00 午餐
论坛主持:杨建红,主任药师,前CDE
- 13:00 中美药品专利链接制度比较
杨建红,主任药师,前CDE
- 13:45 国药品专利纠纷早期解决机制实施办法解读与实务探讨
刘雷,知识产权管理中心执行总监,江苏恩华药业
14:30 茶歇
- 15:00 国内药企进入美国:商业模式与法律考量
陈少羽,上海办公室管理合伙人,美国凯寿律师事务所
- 15:45 小组讨论:如何利用药品专利链接制度
孔祥生 ,总裁助理, 丽珠医药集团
窦夏睿,知识产权总监,扬子江药业集团
陈少羽,上海办公室管理合伙人,美国凯寿律师事务所
- 16:30 会议结束
12月7日(周二)
论坛主持:叶英,董事长,力品药业(厦门)股份有限公司
- 13:30 改良型创新研发中的风险及其控制
赵大川,首席科学官,越洋医药
- 14:30 长效局麻改良型新药中美研发策略研究
陈柏州,CEO,加立生物科技有限公司
15:30 茶歇
- 16:00 改良型创新505B2法规解读,研发立项,临床及注册要点
刘志,制剂研究院副院长,华海药业
- 17:00 小组讨论:中国药企全球化布局的关键问题-立项评估流程CMC、注册策略规划成本市场和收益
叶英,董事长,力品药业(厦门)股份有限公司
赵大川,首席科学官,越洋医药
陈柏州,CEO,加立生物科技有限公司
- 17:45 会议结束
12月8日(周三)
论坛主持:赵大川,首席科学官,越洋医药
- 08:30 505b2产品的立项准备和临床研究流程-FDA法规CMC要求;研发关键;注册要点
陈永奇,董事长,珠海瑞思普利
- 09:30 儿童制剂与规格改良
赵志刚,药学部主任 ,首都医科大学附属北京天坛医院
- 10:30 茶歇
- 11:00 全球专利布局、专利及数据保护、解析及案例分享
耿文军,副总裁,正大天晴药业
12:00 午餐
论坛主持:王龙,注册和商务副总裁,上海奥全生物医药
- 13:00近年来全球重要市场505(b)2批准和研究情况及前瞻
梅兴国,教授,军事医学研究院毒物药物研究所
- 13:45 505b2类药物申报之非临床研究(技术要求,Hybrid between NDA,及案例分析)
王龙,注册和商务副总裁,上海奥全生物医药
14:30 茶歇
- 15:00 前药技术在口服505(b)(2)产品中的应用
向家宁,创始人兼首席科学官,凯瑞康宁
- 15:45 小组讨论:什么样的品种和市场适合改良型创新和主要市场申报
- 梅兴国,教授,军事医学研究院毒物药物研究所
- 王龙,注册和商务副总裁,上海奥全生物医药
- 陈永奇,董事长,珠海瑞思普利
- 16:30 会议结束
12月7日(周二)
论坛主持:刘万卉,副总裁,绿叶制药
- 13:30 药物创新的偏门-复杂注射剂能够极大提升小分子药物的临床和投资价值(45m)
何军,研究员,药物制剂国家工程研究中心
- 14:30 超临界结晶技术在脂质体递送中的应用(30m)
胡勇刚,首席科学家,普萃超临界
- 15:00 无菌喷雾干燥:注射用粉剂的下一篇章(45m)
赵俊兴,首席科学家,浙江医药
15:30 茶歇
- 16:00 微球制剂前景分析及产业化
刘万卉,副总裁,绿叶制药
- 17:00 小组讨论:仿创复杂注射剂开发常见问题及解决方法
刘万卉,副总裁,绿叶制药
赵俊兴,首席科学家,浙江医药
胡勇刚,首席科学家,普萃超临界
- 17:45 会议结束
12月8日(周三)
论坛主持:徐宇虹,创始人,杭州高田生物
- 08:30 纳米脂质体创新药开发及临床药代分析
徐宇虹,创始人,杭州高田生物
- 09:30 艾博生物的高体内活性阳离子脂质在核酸递送系统中的应用
张志一,制剂副总裁,艾博生物
10:30 茶歇
- 11:00 脂质体递药技术在新药开发中的应用
吕万良,教授,北京大学
12:00 午餐
论坛主持:陈涛,总裁,西安力邦制药
- 13:00 PLGA微球缓释注射液的体外/体内相关性
金拓,合作创始人,百剂博递
- 13:45 原位凝胶长效缓释制剂处方筛选与评价
陈涛,董事长,西安力邦制药
14:30 茶歇
- 15:00 体内植入长效制剂的开发
王震宇,副总经理/研究院院长,四川普锐特药业
- 15:45 小组讨论:复杂注射剂的特点及开发难度探讨
陈涛,总裁,西安力邦制药
王震宇,副总经理/研究院院长,四川普锐特药业
徐宇虹,创始人,杭州高田生物
霍秀敏,主任药师,高级审评员,前CDE
- 16:30 会议结束
12月7日(周二)
论坛主持:全丹毅,所长,江苏集萃新型药物制剂技术研究所
- 13:30 国家药审中心《皮肤外用药研究技术指南》起草背景及解读
张星一,高级审评员,前CDE
- 14:30 《化学仿制药透皮贴剂技术指导原则》解析及透皮制剂立项依据和技术挑战
全丹毅,所长,江苏集萃新型药物制剂技术研究所
15:30 茶歇
- 16:00 从FDA积极获批的皮肤局部复杂制剂中获得的研发思考与案例分享
罗华菲,研究员,药物制剂国家工程研究中心
- 17:00 小组讨论:国内外透皮贴剂的研发趋势及面临的难点探讨
全丹毅,所长,江苏集萃新型药物制剂技术研究所
张星一,高级审评员,前CDE
罗华菲,研究员,药物制剂国家工程研究中心
- 17:45 会议结束
12月8日(周三)
论坛主持:汪晴,药学系主任,大连理工大学
- 08:30 透皮制剂的开发 - 从实验室筛选到产业化
章新,董事长,鑫稳生物科技
- 09:30 透皮给药系统为患者提供更好的治疗效果,为健康而创新(30m)
Stefan Arnold,亚洲业务发展总监,LTS
10:30 茶歇
- 11:00 透皮给药辅料的可及性-开发及应用
涂家生,教授,中国药科大学
12:00 午餐
论坛主持:杨永胜,资深副总裁,浙江海昶
- 13:00 透皮贴剂的体外药物释放、体外皮肤渗透和黏附性
汪晴,药学系主任,大连理工大学
- 13:45 皮肤局部用药的生物等效性研究以及监管考量
杨永胜,资深副总裁,浙江海昶
14:30 茶歇
- 15:00 透皮给药处方工艺开发
汤秀珍,研发总监,上海复耀医药
- 15:45 小组讨论:新技术新方法在透皮给药中的应用
汪晴,药学系主任,大连理工大学
杨永胜,资深副总裁,浙江海昶
汤秀珍,研发总监,上海复耀医药
- 16:30 会议结束
Part 5
第三届创新药国际峰会
12月9-10日(周四~周五)
主办方致欢迎词
- 08:30 创新药物研发中的新趋势和新技术
回爱民,执行总裁,复星医药
- 09:15 新发展形势下创新药CMC面临的挑战和思考
杜争鸣,高级副总裁,百济神州
10:00 茶歇
- 10:30 创新药开发过程中的一些思考
吴振平,高级副总裁,和记黄埔
- 11:15 圆桌讨论:新药开发中的挑战与机遇
吴振平,高级副总裁,和记黄埔
温剑锋,高级副总裁,亚盛医药
杜争鸣,高级副总裁,百济神州
回爱民,执行总裁,复星医药
党群,总裁,河南真实生物
刘艳玮,副总裁,注册事务部负责人,武田中国
12:05 午餐
论坛主持:周文来,高级副总裁,加科思
- 13:30 小分子创新药研发:从靶点评估到临床所面临的挑战与机遇(45m)
兰炯, 首席执行官,劲方医药
- 14:15 化学空间(Chemical Space)理论下的多肽创新药的智能药物设计(30m)
何润泽,董事长,上海胜普泽泰医药
- 14:45 克服靶向癌症治疗耐药性的关键(45m)
周文来,高级副总裁,加科思
15:30 茶歇
- 16:00 强透脑BTK抑制剂的开发
原晨光,资深副总裁,成都海博为药业
- 17:00 小组讨论:人工智能、新靶点、新技术在抗肿瘤药物研发中的应用进展探讨
原晨光,资深副总裁,成都海博为药业
周文来,高级副总裁,加科思
党群,总裁,河南真实生物
- 17:45 会议结束
12月10日(周五)
论坛主持:马连东,副总裁,开拓药业
- 08:30 前药技术在发现BIC药物中的应用
党群,总裁,河南真实生物
- 09:30 基于质谱的亲合性筛选在药物发现中的应用
邓永奇,董事长/ 总经理,凯复生物
10:30 茶歇
- 11:00 下一代抗癌药物发现: 难成药靶点蛋白质降解剂的研发
马连东,副总裁,开拓药业
12:00 午餐
论坛主持:崔海峰,首席科学家,济民可信集团研发中心
- 13:00 如何减少药物发现周期和降低研发成本?
习宁 ,总裁,北京范恩柯尔生物
- 13:45 用于RNA治疗的新型药物递送平台
王海盛,副总裁,哈药集团
14:30 茶歇
- 15:00 创新性小分子研发的思考
崔海峰,首席科学家,济民可信集团研发中心
- 15:45 小组讨论:创新药研发靶点走向同质化,如何突破药物创新困局?
崔海峰,首席科学家,济民可信集团研发中心
王海盛,副总裁,哈药集团
马连东,副总裁,开拓药业
-
16:30 会议结束
12月9日(周四)
论坛主持:顾虹,总经理,上海奥博生物医药
- 13:30 新药研发中原料药杂质的评估检测和控制(45m)
顾虹,总经理,上海奥博生物医药
- 14:30 AI赋能小分子药物合成与工艺设计(30m)
曾琢, 创始人,苏州沃时数字科技
- 15:00 原料药关键质量属性参数的确定和控制(45m)
李洪明,首席运营官,福建广生堂
- 15:30 茶歇
- 16:00 多组分原料药的质控研究
余立,主任药师,北京食品药品检验所
- 17:00 小组讨论:应用风险评估理念科学合理的控制药物中的杂质
顾虹,总经理,上海奥博生物医药
李洪明,首席运营官,福建广生堂
余立,主任药师,北京食品药品检验所
- 17:45 会议结束
12月10日(周五)
论坛主持:陆国浩,副总监,USP
- 08:30 满足全球申报新药不同开发阶段的稳定性设计和研究
李文叶,高级总监,康龙化成
- 09:30 原料药起始物料的选择依据(30m)
张唐志,高级副总裁,上海凌凯医药
- 10:00 原料药固态研究及控制技术(30m)
杨建海, 原料药开发总监,杭州领业
10:30 茶歇
- 11:00 美国药典杂质控制策略
陆国浩,副总监,USP
- 12:00 午餐
论坛主持:龚俊波,教授,天津大学
- 13:00 原料药中基因毒杂质的研究策略和控制手段
吴恺,CMC副总监,强生制药
- 13:45 新药研发中的化学工艺优化
汪有初,副总裁,合全药业
14:30 茶歇
- 15:00 原料药晶型的筛选,优势晶型的确定和分析,结晶工艺的研究
龚俊波,教授,天津大学
- 15:45 小组讨论:在新药开发过程中,如何选择原料药工艺和进一步优化?
吴恺,CMC副总监,强生制药
汪有初,副总裁,合全药业
龚俊波,教授,天津大学
- 16:30 会议结束
12月9日(周四)
论坛主持:陈霖,研发总监,Bayer
- 13:30 新型治疗实体的药物递送(45m)
陈霖,研发总监,Bayer
- 14:15 QbD理念在新药制剂研发中的应用(45m)
韩军,院长,聊城大学生物制药研究院
- 15:00 自动化高通量制剂筛选平台助力制剂设计与研发(30m)
曹露,自动化客户经理,Unchained Labs
15:30 茶歇
- 16:00 临床前处方开发需要考虑的因素
刘恒利, 高级总监,凯信远达研发中心
- 17:00 小组讨论:创新药的制剂研究需要关注的问题有哪些?
陈霖,研发总监,Bayer
韩军,院长,聊城大学生物制药研究院
刘恒利, 高级总监,凯信远达研发中心
- 17:45 会议结束
12月10日(周五)
论坛主持:韩军,院长,聊城大学生物制药研究院
- 08:30 喷雾干燥技术在制剂产品中的应用
Deepak Hegde,CTO,EOC Pharma
- 09:30 提高创新药制剂研发效率的考量
吴振平,高级副总裁,和记黄埔
- 10:30 茶歇
- 11:00 OM 缓释片剂 IVIVC 开发
毕明达,集团副总裁,朗华制药
12:00 午餐
- 13:00 临床三期至商业化生产阶段处方工艺开发
张磊,pCMC制剂研发负责人,罗氏
- 13:45 长效缓释注射剂助力新药研发
罗亮,董事长&首席科学家,武汉百纳礼康生物制药有限公司
14:30 茶歇
- 15:00 临床前处方毒理学研究
胡怀忠,首席科学官,成都创宜生物
- 15:45 小组讨论:创新药制剂选择剂型的考虑要点及策略探讨
罗亮,董事长&首席科学家,武汉百纳礼康生物制药有限公司
胡怀忠,首席科学官,成都创宜生物
张磊,pCMC制剂研发负责人,罗氏
- 16:30 会议结束
12月9日(周四)
论坛主持:陈勇,副总裁,康龙化成
- 13:30 从COVID-19中汲取的经验教训,以支持CMC运营的CMC分析开发和质量控制,全球视角看分析化学在新药开发中的新角色
陈勇,副总裁,康龙化成
- 14:30 基于QbD理念的分析方法开发-验证-转移
高青,主任药师,北京市药品检验鉴定研究所
15:30 茶歇
- 16:00 创新药基因毒性杂质的研究
刘学明,执行总监,百济神州
- 17:00 小组讨论:全球范围内的临床早期开发与晚期开发对数据完整性的挑战
陈勇,副总裁,康龙化成
高青,主任药师,北京市药品检验鉴定研究所
刘学明,执行总监,百济神州
- 17:45 会议结束
12月10日(周五)
论坛主持:刘学明,执行总监,百济神州
- 08:30 原料药分析检测方法的建立,如何做到充分满足注册申报要求?
梁睿颋,ARD总监,百济神州
- 09:30 质谱成像新技术与中枢神经系统药物研发
贺玖明,研究员,中国医学科学院药物研究所
10:30 茶歇
- 11:00 分析方法开放及生命周期管理(Q14)
奚凤德,首席科学家,京新药业,前USP美国副总裁
12:00 午餐
论坛主持:房杏春,副总经理,重庆两江药物研发
- 13:00 新药研发中的质量标准、稳定性、变更桥接策略
张晞晨,生产高级副总裁, 创胜集团
- 13:45 分析团队在新药研发过程面临的挑战-案例分享
崔立杰,分析化学部副总经理 ,凯莱英医药集团
14:30 茶歇
- 15:00 产品开发中的分析研发与控制
房杏春,副总经理,重庆两江药物研发
- 15:45 小组讨论:新药开发过程中方法,质量标准及标准品建立的挑战
梁睿颋,ARD总监,百济神州
房杏春,副总经理,重庆两江药物研发
崔立杰,分析化学部副总经理 ,凯莱英医药集团
-
16:30 会议结束
12月9日(周四)
论坛主持:刘艳玮,副总裁,注册事务部负责人,武田中国
- 13:30 国内最近的法规变化
曹海峰,副总裁,法规及药学开发部负责人, 瑞石生物
- 14:30 新法规下加速新药审评审批的实践分享
刘艳玮,副总裁,注册事务部负责人,武田中国
15:30 茶歇
- 16:00 肿瘤真实世界研究在新政策法规下的应用
郭彤,执行副总裁,零氪科技
- 17:00 小组讨论:新法规下创新药研发策略探讨
刘艳玮,副总裁,注册事务部负责人,武田中国
张瑾,总监,百济神州
左珺,副总裁,和铂医药
- 17:45 会议结束
12月10日(周五)
论坛主持:李娅杰,副总裁,精鼎医药
- 08:30 使用国外数据进行药物开发
肖申,首席战略官,思路迪医药
- 09:30 与药监机构的沟通交流
熊善丽,执行总监,百济神州
10:30 茶歇
- 11:00 Q12面临的CMC监管挑战与科学技术的创新
吴正宇,注册总监,诺和诺德
12:00 午餐
- 13:00 监管环境变化:基于临床需求的药品研发及审评审批
李娅杰,副总裁,精鼎医药
- 13:45 中美伴随诊断监管政策与注册申报策略
陶源,副总裁,罗氏诊断
14:30 茶歇
- 15:00 临床阶段美国FDA对CMC的要求及案例分析
王勇,副总裁,DataRevive LLC
- 15:45 小组讨论:创新药如何通过加快上市获批?
李娅杰,副总裁,精鼎医药
陶源,副总裁,罗氏诊断
熊善丽,执行总监,百济神州
- 16:30 会议结束
12月9日(周四)
论坛主持:刘东舟,首席科学官,华东医药
- 13:30 新药临床方案设计
刘平,首席医学官,福贝医药
- 14:30 抗肿瘤药物市场现状和研发趋势
房良华,执行总监,齐鲁制药
15:30 茶歇
- 16:00 对当前创新药临床研发若干问题的一些思考
黄钦,高级副总裁,先声药业
- 17:00 小组讨论:新政策环境下如何识别和评估创新药物临床试验风险
刘东舟,首席科学官,华东医药
黄钦,高级副总裁,先声药业
刘平,首席医学官,福贝医药
- 17:45 会议结束
12月10日(周五)
论坛主持:华烨,董事长,烨辉医药
- 08:30 临床研究中药物安全风险管理的考量和建议
磨筱垚,创始人,北京信安佳康医疗科技有限公司
- 09:30 I期临床研究的目标
张大为,总经理,江苏迈度药物
10:30 茶歇
- 11:00 临床研究中的概念验证
赵冰,首席医学官,徐诺药业
12:00 午餐
论坛主持:郭晓宁,首席医学官,赛生药业
- 13:00 在未满足的临床需求前提下来快速开发新药
华烨,董事长,烨辉医药
- 13:45 以临床价值为导向,早期PK/PD研究在创新药整体研发链条中的重要价值
刘波, 教授,武汉工程大学
14:30 茶歇
- 15:00 抗病毒药物临床试验中的临床药理考虑
丁俊杰,总监,阿斯利康
- 15:45 小组讨论:创新药早期临床研究之路如何走-从策略,试验设计到实施
郭晓宁,首席医学官,赛生药业
丁俊杰,总监,阿斯利康
刘波, 教授,武汉工程大学
张大为,总经理,江苏迈度药物
- 16:30 会议结束









文章评论(0)