2021年全球畅销药物TOP10,最高超240亿美元
其中,辉瑞/BioNtech生产的BTN162b2仍以243亿美元的销售额稳居第一,艾伯维的Humira(修美乐)及默沙东的Keytruda(帕博利珠单抗)则分别以153.6亿美元、125.78亿美元位居榜单第2、3名。
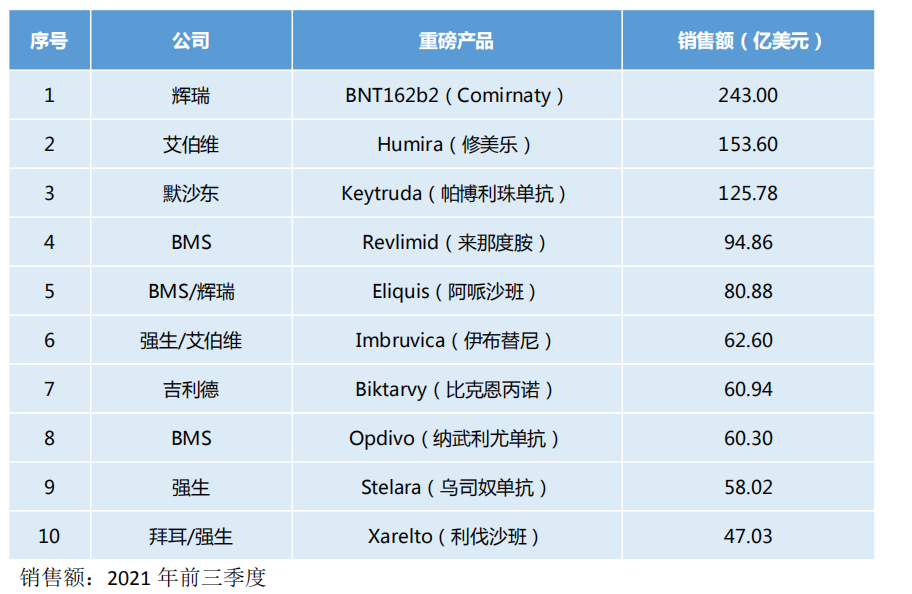
以下为2021年全球畅销药物TOP10具体内容(仅供参考):
临床数据显示,辉瑞疫苗防重症95%,防出现症状96%,但如果有三个以上并发症(肥胖、高血压、糖尿病、心脏病、肾病、神经系统疾病、免疫缺失等),则有效率降到88%。
此外,辉瑞还进行了第三针疫苗的临床试验,初步数据显示:在接种第二剂6个月之后接种第三剂增强疫苗,中和抗体滴度比二针剂提高5-8倍;针对Beta变种(B.1.351),中和抗体滴度比二针剂提高15-21倍;针对近来流行的Delta变种,中和抗体滴度在18-55岁成人中提高5倍以上,在65-80岁老年人中提高11倍以上。
截至目前,Humira在美国、欧盟和日本获批用于成人中重度慢性类风湿性关节炎和儿童多关节少年特发性关节炎、银屑病和银屑病关节炎、强直性脊柱炎、儿童和成人克罗恩病、溃疡性结肠炎(仅限美国和欧盟)等。此外,Humira正在进行结节病和葡萄膜炎治疗的临床试验。
不过,2023年Humira将在美国失去专利保护,对其销售额可能会产生一定的影响。
2017年,FDA批准Keytruda上市用于治疗微卫星不稳定的实体瘤;2018年7月,Keytruda(帕博利珠单抗)获得国家药品监督管理局批准正式在中国上市,用于一线治疗后疾病发生进展的局部晚期或转移性黑色素瘤,成为继Opdivo之后第2个在中国上市的PD-1/PD-L1单抗药物。虽然在国内上市较Opdivo晚,但Keytruda凭借其广泛的适应症已将Opdivo远远甩在身后。
截至目前,Keytruda已获批用于非小细胞肺癌(中国)、小细胞肺癌、肝癌、肾癌、胃癌、宫颈癌、子宫内膜癌、食管癌、黑色素瘤(中国)、头颈部鳞癌、霍奇金淋巴瘤、尿路上皮癌、原发性纵隔大B细胞淋巴瘤、MSI-H实体瘤、默克细胞癌、TMB-H实体瘤、皮肤鳞状细胞癌、MSI-H/dMMR结直肠癌、三阴性乳腺癌等超过25种适应症,成为名副其实的抗癌“神药”。
据EvaluatePharma分析报告指出,Keytruda预计将在2023年取代艾伯维的Humira,成为世界上最畅销的药物,且有望2026年全球销售额达到243.2亿美元。
2006年,FDA批准Revlimid上市用于多发性骨髓瘤(MM)的治疗,目前临床主要用于治疗多发性骨髓瘤、套细胞淋巴瘤和有5q缺失的骨髓增生异常综合症。Revlimid也是国内治疗多发性骨髓瘤的一线药物,可有效抑制癌症的进一步扩散和转移。
据悉,2019年百时美施贵宝通过重金收购新基获得Revlimid,预计2025年该药销售额将超124亿美元,但与此同时,也将迎来专利悬崖。
目前,除美国、欧洲、加拿大和日本外,Eliquis已在包括韩国、印度、马来西亚、菲律宾、新加坡、香港及台湾等45个国家和地区正式批准用于房颤卒中和体循栓塞预防。此外,心脑血管疾病是全球第一大死因,我国因心脑血管疾病所致死亡者占死亡总人数的45%,每年因心脑血管疾病死亡人数达260万,平均每小时死亡340人。
基于此,Eliquis在2025年的销售额预计将达到120亿美元。
自2013年首次获得批准上市以来,Imbruvica已获批套细胞淋巴瘤、边缘区淋巴瘤、小细胞淋巴瘤、CLL、WM在内的5种B细胞血液癌症以及包括慢性移植物抗宿主病在内总共6种疾病领域。2017年,Imbruvica获得国家药品监督管理局批准,可作为单药用于CLL/SLL患者以及既往至少接受过一种治疗的MCL患者的治疗,中文商品名为亿珂。
在2018医保谈判中,Imbruvica通过大幅降价成功进入医保目录,该药在2025年的销售额预计将达119亿美元。
2018年Biktarvy在美国获批上市,可作为一种完整方案,用于治疗HIV-1感染的儿科患者(体重≥14公斤)和成人患者,这些患者无治疗失败史,并且不存在已知的对Biktarvy每个组份耐药相关的突变。随后,Biktarvy也在国内获批上市,适用于作为完整方案治疗人类免疫缺陷病毒1型(HIV-1)感染的成人。
自2014年7月获批以来,纳武利尤单抗已在60多个国家和地区获批治疗十余个癌种,涵盖肺癌、头颈癌、胃癌、食管癌、肝癌、肾癌、结直肠癌、尿路上皮癌、黑色素瘤、霍奇金淋巴瘤、胸膜肿瘤等。
虽是全球首个PD-1产品,近几年,随着 Keytruda适应症的不断拓展,Opdivo的销售额甚至出现负增长。此外,今年7月,Opdivo与索拉非尼一线治疗肝癌的总生存期主要终点没有达到统计学意义,BMS也不得已向FDA撤回该项适应症的上市申请。
2009年,Stelara首次获FDA批准用于中度至重度斑块型银屑病成人患者。在临床上,Stelara已成为一种广泛认可的中重度银屑病标准治疗药物。目前,Stelara已获全球多个国家批准用于中度至重度斑块型银屑病、活动性银屑病关节炎及克罗恩病的治疗。
目前,Xarelto在美国获批九种适应症,是所有直接口服抗凝剂(DOAC)中适应症最多的一种。且是第一种也是唯一一种有助于降低冠心病(CAD)患者主要心血管(CV)事件和主要血栓性血管事件风险的治疗方法,如心肌梗死、缺血性中风、急性肢体缺血和血管性疾病的主要截肢,PAD患者,包括最近因症状性PAD而接受LER的患者。
据EvaluatePharma预测,Xarelto在2024年的全球销售额将达到59.15亿美元,其中美国市场将达到43.02亿美元。


文章评论(0)