3月License报告 | 6起19亿,单抗出海,肿瘤药物上市,涉及百济、信达、科兴…
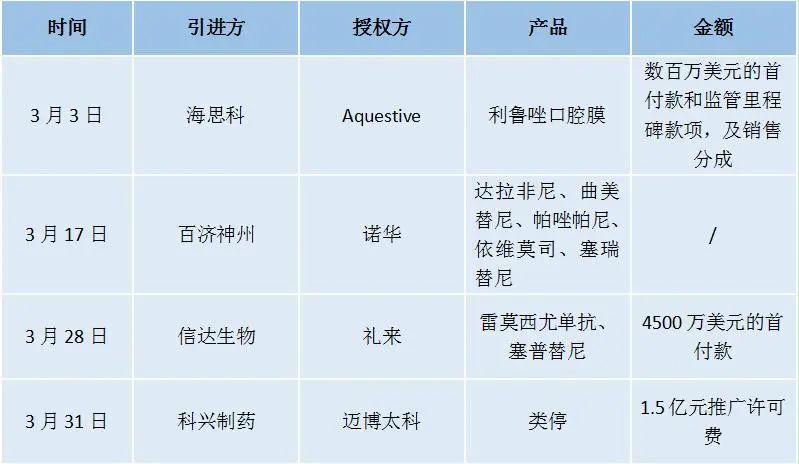
2022年3月国内药企license交易一览
License in
海思科数百万美元布局ALS领域
根据协议,Aquestive可获得数百万美元的首付款和监管里程碑款项,及销售分成。
据悉,利鲁唑口腔膜是Aquestive通过其PharmFilm创新药物递送技术开发的口服薄膜制剂,已于2019年11月获得FDA批准上市,用于治疗肌萎缩侧索硬化症(ALS)。该产品无需液体或食物即可迅速溶解,其剂型的特殊性将为吞咽困难或者无法吞咽的ALS患者提供有意义的治疗选择。
据悉,这5款产品包括BRAF抑制剂泰菲乐®(达拉非尼)、MEK抑制剂迈吉宁®(曲美替尼)、VEGFR抑制剂维全特®(帕唑帕尼)、mTOR抑制剂飞尼妥®(依维莫司)以及ALK抑制剂赞可达®(塞瑞替尼),目前均已在国内获批上市并被纳入医保目录。
根据协议,信达生物将支付礼来总计4500万美元的首付款,并负责这2款重磅靶向新药在中国的销售。
据悉,希冉择(雷莫西尤单抗)是FDA批准的首个针对化疗后晚期或转移性胃或胃食管结合部(GEJ)腺癌患者的治疗方案,也是FDA批准的首个针对晚期肝细胞癌(HCC)患者的生物标记物驱动疗法。目前,希冉择用于晚期胃或胃食管结合部腺癌的适应症已获NMPA批准上市,成为国内首个且唯一一个被批准用于晚期胃癌二线治疗的靶向药物,且肝细胞癌的二线疗法新适应症也处于上市申请阶段。
根据协议,迈博太科可获得1.5亿元推广许可费,含5000万元首付款。
据悉,2021年7月,NMPA已批准注射用英夫利西单抗(类停)上市,主要用于类风湿关节炎、银屑病、强直性脊柱炎、成人溃疡性结肠炎、成人及儿童克罗恩病及瘘管性克罗恩病的治疗,是国内首个上市的英夫利西单抗生物类似药。
License out
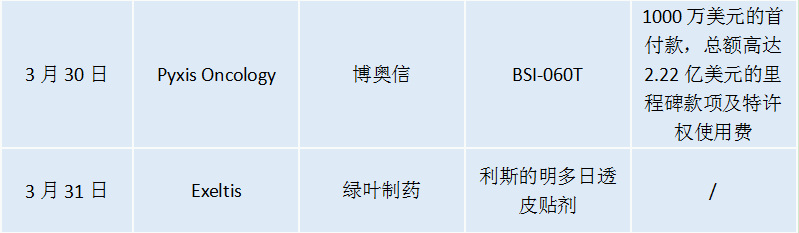
根据协议,博奥信可获得1000万美元的首付款,总额高达2.22亿美元的里程碑款项及销售额中高达两位数比例的特许权使用费。
据悉,BSI-060T属于抗Siglec-15单抗,临床前研究显示,与对标药物相比,BSI-060T具有更高的亲和力、更强的生物活性,以及更长的半衰期,有望成为治疗实体瘤的同类最优抗体。
据悉,利斯的明多日透皮贴剂是一周两次的新贴剂剂型,用于治疗与阿尔茨海默病相关的轻、中度痴呆症。该产品由绿叶制药专有的透皮释药技术平台开发,已在欧洲多个国家获得上市许可。
近年来,在创新药相关政策及医保的推进下,抗肿瘤新药成为各药企抢占市场的关键,以百济神州与信达生物为代表的本土创新药企业,一方面通过自研完善相关产品管线,另一方面加紧通过引进弥补自身不足。
当然,随着更多新药获批上市,对国内患者而言将拥有更多的选择空间。


文章评论(0)